O ozônio age em microrganismos criando furos na prede celular que é vital para uma bactéria ou bacilo, o ozônio rompe a parede celular matando a célula. Quando uma célula se estressa por ataque de fungos, vírus ou bactérias, seu nível de energia é reduzido pela fuga de elétrons e ela se torna eletropositiva. Nessa condição em um nível molecular, os elétrons que fogem, são chamados de elétrons livres, que é o mesmo que dizer que estão mais distantes do núcleo do átomo. O ozônio tem um pequeno elétron livre com carga elétrica no terceiro átomo de oxigênio que procura equilibrar-se eletricamente com outro material, microrganismo com uma carga elétrica negativa correspondente não equilibrada. Ao reagir com microrganismos, poluentes, volta ao seu estado natural: o oxigênio (O2). Células doentes, vírus, bactérias perigosas e outras patogenias carregam essa carga negativa e atraem ozônio e seus derivados. Células de saúde normal não conseguem reagir com ozônio ou seus derivados, já que possuem carga elétrica equilibrada e um sistema de enzimas forte.
Por que uma célula morre com o ozônio?
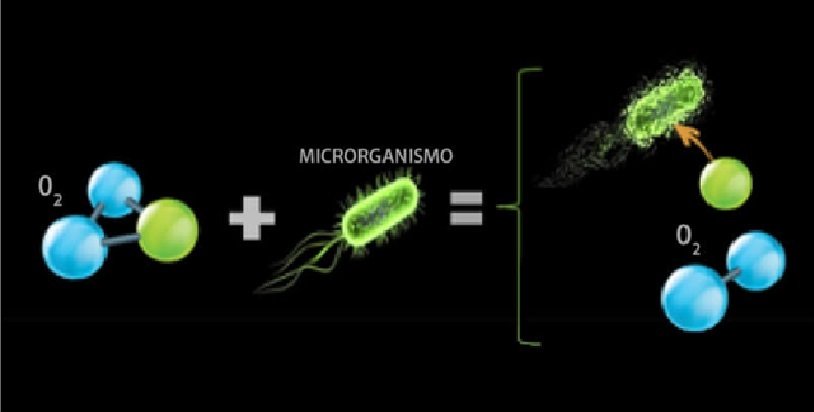
Processo de inativação de microrganismo
O processo de inativação do microrganismo por ozônio é complexo. Ele ataca as membranas e os constituintes das paredes de diversas células e também o conteúdo da célula. Tanto o ozônio molecular como os radicais livres produzidos pelo seu colapso têm um papel importante neste processo. O microrganismo é morto devido à ruptura ou desintegração da membrana da parede celular, levando à dispersão dos conteúdos da célula. Cada microrganismo tem uma sensibilidade diferente em relação ao ozônio. As bactérias são mais sensíveis do que os fungos e leveduras. Bactérias gram-positivas são mais sensíveis ao ozônio do que organismos gram-negativos, e esporos são mais resistentes do que células vegetativas. Por seu mecanismo de ação que destrói o microrganismo através da dissolução da célula, ele não permite a resistência do mesmo.
Como o Ozônio age em microrganismos: destruindo uma bactéria

1 – Uma célula bacteriana de bacilo.
2 – O ozônio entra em contato com a parede celular que é vital para a bactéria.
3 – À medida que as moléculas de ozônio fazem contato com a parede celular, o poder oxidativo do ozônio rompe a parede celular criando um pequeno orifício na célula.
4 – Um furo recém-criado na parede celular prejudicou a bactéria.
5 – A bactéria começa a perder a sua forma enquanto as moléculas de ozônio continuam a criar furos na parede celular.
6 – Após milhares de colisões de ozônio em apenas alguns segundos, a parede bacteriana não pode mais manter sua forma e a célula morre.
Nota: A oxidação de células bacterianas via contato de ozônio ocorre de 1 à 10 segundos.
Importante
O efeito do ozônio abaixo de um valor correto de concentração é pequeno ou nulo. Acima deste nível, todos os agentes patogênicos são eventualmente destruídos.
Caracteristicas do ozônio
O gás ozônio possui um elevado potencial oxidativo que o destaca como um excelente “destruidor” de compostos orgânicos e de patógenos. O potencial oxidativo do ozônio é de aproximadamente 2,07 mV, enquanto o cloro, por exemplo, é de aproximadamente 1,36 mV (ver Tabela 1). Já o flúor possui um potencial de aproximadamente 3,06 mV.
Este elevado poder de oxidação do ozônio confere uma elevada capacidade na remoção de matéria orgânica e na desinfecção da água bruta, com um menor tempo de contato e menores concentrações, tornando o uso do ozônio como um potencial oxidante em estações de tratamento de esgoto e água. Por ser um gás instável, o ozônio possui um tempo de meia vida curto (aproximadamente 20,0 minutos em água a 20,0°C), é parcialmente solúvel em água e, assim como a maioria dos gases, aumenta sua solubilidade à medida que a temperatura diminui. A solubilidade do ozônio na água dependerá da concentração de matéria orgânica presente, pois quanto menor a concentração de matéria orgânica, maior será o tempo de meia vida do ozônio em água (FERREIRA, 2017 apud WYSOK et al., 2006).
A decomposição do ozônio em meio aquoso é caracterizada por uma rápida diminuição da concentração inicial, com uma fase posterior na qual a concentração de ozônio diminui segundo uma cinética de primeira ordem, sendo que os radicais hidroxila (OH) são os principais produtos desta decomposição. O ozônio pode reagir com compostos orgânicos em solução aquosa através da reação direta, onde o próprio ozônio molecular atua; e, através da reação indireta, na qual envolve reações com os radicais hidroxila (OH), formados da decomposição do ozônio em meio aquoso. A reação indireta não é seletiva, pois ela é capaz de promover um ataque a compostos orgânicos 106 – 109 vezes mais rápido que alguns agentes oxidantes como, por exemplo, o peroxido de hidrogênio (H2O2) e o próprio ozônio. Predominantemente processos de desinfecção ocorrem via ozônio molecular, já processos de oxidação podem ocorrer tanto por meio do ozônio molecular, via direta, como dos radicais hidroxila, via indireta (ALMEIDA et al., 2004; DI BERNADO e DANTAS, 2005; SILVA et al., 2011).
A formação de radicais hidroxila (OH) leva à rápida decomposição do ozônio em meio aquoso e assim como outros compostos oxidantes, aumentando os níveis de pH. As alterações na eficiência do processo de desinfecção, quando há uma representativa variação no pH do meio, relacionam-se com mudanças na taxa de decomposição do ozônio. Segundo Kim et al., (1998) citado por Ferreira (2017), a estabilidade do ozônio em água decresce quando o pH do meio aumenta; quando esse pH é superior a 8,0 praticamente metade do ozônio introduzido é decomposto em várias formas intermediárias de oxigênio, num período de 10,0 minutos.


